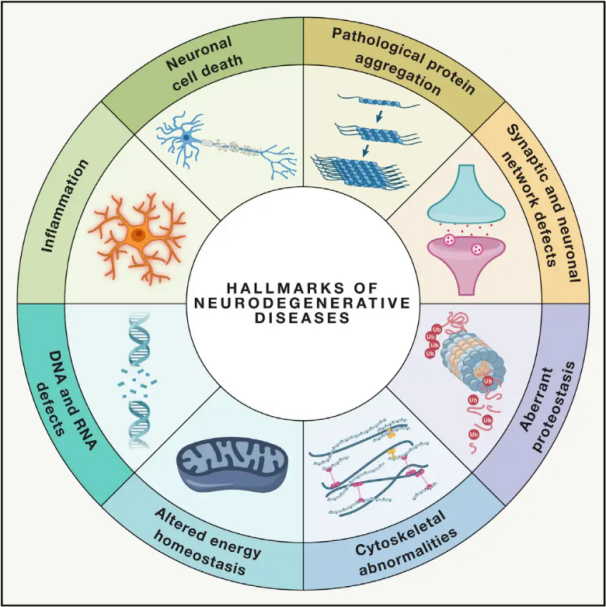
Enfermidades neurodexenerativasAs EDN caracterízanse pola perda progresiva ou persistente de poboacións neuronais vulnerables específicas dentro do cerebro ou da medula espiñal. A clasificación das EDN pode basearse en varios criterios, incluíndo a distribución anatómica da neurodexeneración (como trastornos extrapiramidais, dexeneración frontotemporal ou ataxias espinocerebelosas), anomalías moleculares primarias (como amiloide-β, prións, tau ou α-sinucleína) ou características clínicas principais (como a enfermidade de Parkinson, a esclerose lateral amiotrófica e a demencia). A pesar destas diferenzas na clasificación e presentación dos síntomas, trastornos como a enfermidade de Parkinson (EP), a esclerose lateral amiotrófica (ELA) e a enfermidade de Alzheimer (EA) comparten procesos subxacentes comúns que levan á disfunción neuronal e á eventual morte celular.
Con millóns de persoas en todo o mundo afectadas por trastornos neurodexenerativos (EDN), a Organización Mundial da Saúde estima que para 2040 estas enfermidades converteranse na segunda causa de morte nos países desenvolvidos. Aínda que existen varios tratamentos dispoñibles para aliviar e controlar os síntomas asociados a enfermidades específicas, os métodos eficaces para frear ou curar a progresión destas afeccións seguen sendo difíciles de atopar. Estudos recentes indican un cambio nos paradigmas de tratamento, pasando do mero tratamento sintomático á utilización de mecanismos de protección celular para evitar un maior deterioro. As amplas evidencias suxiren que o estrés oxidativo e a inflamación desempeñan papeis fundamentais na neurodexeneración, o que posiciona estes mecanismos como obxectivos críticos para a protección celular. Nos últimos anos, a investigación fundamental e clínica revelou o potencial da terapia de osíxeno hiperbárico (OTHB) no tratamento de enfermidades neurodexenerativas.
Comprender a terapia de osíxeno hiperbárico (OTHB)
A OHB adoita implicar aumentar a presión por riba dunha atmosfera absoluta (ATA) (a presión ao nivel do mar) durante unha duración de 90 a 120 minutos, o que a miúdo require varias sesións dependendo da afección específica que se estea tratando. A presión de aire mellora a subministración de osíxeno ás células, o que á súa vez estimula a proliferación das células nai e potencia os procesos de curación mediados por certos factores de crecemento.
Orixinalmente, a aplicación da TOHB baseouse na lei de Boyle-Marriott, que postula a redución das burbullas de gas dependente da presión, xunto cos beneficios dos altos niveis de osíxeno nos tecidos. Existe unha serie de patoloxías coñecidas que se benefician do estado hiperóxico producido pola TOHB, incluíndo tecidos necróticos, lesións por radiación, traumatismos, queimaduras, síndrome compartimental e gangrena gasosa, entre outras enumeradas pola Sociedade Médica Submarina e Hiperbárica. Cabe destacar que a TOHB tamén demostrou eficacia como tratamento adxunto en varios modelos de enfermidades inflamatorias ou infecciosas, como a colite e a sepsis. Dados os seus mecanismos antiinflamatorios e oxidativos, a TOHB ofrece un potencial significativo como vía terapéutica para as enfermidades neurodexenerativas.
Estudos preclínicos da terapia de osíxeno hiperbárico en enfermidades neurodexenerativas: coñecementos do modelo de rato 3×Tg
Un dos estudos máis destacadoscentrouse no modelo murino 3×Tg da enfermidade de Alzheimer (EA), que puxo de manifesto o potencial terapéutico da HBOT para mellorar os déficits cognitivos. A investigación incluíu ratos machos 3×Tg de 17 meses de idade en comparación con ratos machos C57BL/6 de 14 meses de idade que serviron como control. O estudo demostrou que a HBOT non só mellorou a función cognitiva, senón que tamén reduciu significativamente a inflamación, a carga de placa e a fosforilación de Tau, un proceso crítico asociado coa patoloxía da EA.
Os efectos protectores da HBOT atribuíronse a unha diminución da neuroinflamación. Isto evidenciouse pola redución da proliferación microglial, a astrogliose e a secreción de citocinas proinflamatorias. Estes achados salientan o dobre papel da HBOT na mellora do rendemento cognitivo e, ao mesmo tempo, na mitigación dos procesos neuroinflamatorios asociados á enfermidade de Alzheimer.
Outro modelo preclínico utilizou ratos con 1-metil-4-fenil-1,2,3,6-tetrahidropiridina (MPTP) para avaliar os mecanismos de protección da HBOT na función neuronal e as capacidades motoras. Os resultados indicaron que a HBOT contribuía a unha mellora da actividade motora e da forza de agarre nestes ratos, o que se correlacionaba cun aumento da sinalización da bioxénese mitocondrial, concretamente a través da activación de SIRT-1, PGC-1α e TFAM. Isto destaca o papel significativo da función mitocondrial nos efectos neuroprotectores da HBOT.
Os mecanismos da HBOT nas enfermidades neurodexenerativas
O principio subxacente da utilización da HBOT para os trastornos neurodexenerativos (TND) reside na relación entre a redución do subministro de osíxeno e a susceptibilidade a cambios neurodexenerativos. O factor inducible por hipoxia 1 (HIF-1) desempeña un papel central como factor de transcrición que permite a adaptación celular á baixa presión de osíxeno e foi implicado en varios TND, incluíndo a EA, a enfermidade de Parkinson, a enfermidade de Huntington e a ELA, o que o converte nun obxectivo farmacolóxico crucial.
Debido a que a idade é un factor de risco significativo para múltiples trastornos neurodexenerativos, é vital investigar o impacto da HBOT na neurobioloxía do envellecemento. Os estudos indicaron que a HBOT pode mellorar os déficits cognitivos relacionados coa idade en suxeitos maiores sans.Ademais, os pacientes anciáns con deficiencias significativas da memoria mostraron melloras cognitivas e un aumento do fluxo sanguíneo cerebral tras a exposición á HBOT.
1. Impacto da HBOT na inflamación e no estrés oxidativo
A HBOT demostrou a capacidade de aliviar a neuroinflamación en pacientes con disfunción cerebral grave. Posúe a capacidade de regular á baixa as citocinas proinflamatorias (como a IL-1β, a IL-12, o TNFα e o IFNγ) á vez que regula á alza as citocinas antiinflamatorias (como a IL-10). Algúns investigadores propoñen que as especies reactivas de osíxeno (ROS) xeradas pola HBOT median varios efectos beneficiosos da terapia. En consecuencia, ademais da súa acción redutora de burbullas dependente da presión e da consecución dunha alta saturación de osíxeno nos tecidos, os resultados positivos relacionados coa HBOT dependen en parte dos papeis fisiolóxicos dos ROS producidos.
2. Efectos da HBOT na apoptose e a neuroprotección
A investigación indicou que a HBOT pode reducir a fosforilación hipocampal da proteína quinase activada por mitóxenos p38 (MAPK), mellorando posteriormente a cognición e diminuíndo o dano hipocampal. Descubriuse que tanto a HBOT por si soa como en combinación co extracto de Ginkgo biloba reducen a expresión de Bax e a actividade da caspase-9/3, o que resulta nunha diminución das taxas de apoptose en modelos de roedores inducidas por aβ25-35. Ademais, outro estudo demostrou que o preacondicionamento da HBOT induciu tolerancia contra a isquemia cerebral, con mecanismos que implican un aumento da expresión de SIRT1, xunto con niveis aumentados de linfoma de células B 2 (Bcl-2) e unha redución da caspase-3 activa, o que subliña as propiedades neuroprotectoras e antiapoptóticas da HBOT.
3. Influencia da HBOT na circulación eNeuroxénese
A exposición de suxeitos a HBOT asociouse con múltiples efectos no sistema vascular cranial, incluíndo o aumento da permeabilidade da barreira hematoencefálica, a promoción da anxioxénese e a redución do edema. Ademais de proporcionar un maior subministro de osíxeno aos tecidos, a HBOTfavorece a formación vascularmediante a activación de factores de transcrición como o factor de crecemento endotelial vascular e mediante a estimulación da proliferación de células nai neurais.
4. Efectos epixenéticos da HBOT
Os estudos revelaron que a exposición das células endoteliais microvasculares humanas (HMEC-1) ao osíxeno hiperbárico regula significativamente 8.101 xenes, incluíndo expresións tanto reguladas ao alza como á baixa, o que destaca un aumento na expresión xénica asociada ás vías de resposta antioxidante.
Conclusión
O uso da HBOT fixo avances significativos ao longo do tempo, demostrando a súa dispoñibilidade, fiabilidade e seguridade na práctica clínica. Aínda que a HBOT foi explorada como un tratamento non autorizado para os trastornos neuroespecíficos e se realizaron algunhas investigacións, segue a existir unha necesidade urxente de estudos rigorosos para estandarizar as prácticas de HBOT no tratamento destas doenzas. É esencial seguir investigando para determinar as frecuencias óptimas de tratamento e avaliar o grao de efectos beneficiosos para os pacientes.
En resumo, a intersección do osíxeno hiperbárico e as enfermidades neurodexenerativas demostra unha prometedora fronteira nas posibilidades terapéuticas, o que xustifica a exploración e validación continuas en entornos clínicos.
Data de publicación: 16 de maio de 2025

